一、主管机构和核心法规
沙特食品药品管理局 (SFDA) 成立于 2003 年,负责监管食品和药品,以及医疗器械和体外诊断设备。目前使用2008 年第 1-8-1429 号临时法规法令。其定义了“医疗器械”是指制造商打算单独或组合用于人类的任何仪器、装置、器具、机器、植入物、体外试剂或校准器、软件、材料又或其他类似及相关物品 :
l 用于诊断、预防、监测、治疗或缓解疾病;
l 用于诊断、监测、治疗、减轻或补偿伤害/残障;
l 研究、替换、改变或支持生理的解剖结构;
l 支持或维持生命;受孕控制;医疗器械消毒;
二、产品分类
国家食品药品监督管理局(SFDA)推出了医疗器械和产品分类系统(MDC),旨在促进和加快医疗器械和产品分类程序,以电子方式申请注册。在国家食品药品监督管理局及其子部门、海关、港口和其他政府机构的不同部门之间,以及供应商和分销商以及企业医疗器械之间,达到便于管理,高效便捷的目的。
MDS–G42医疗器械指南中,明确沙特将医疗器械分为4类(与欧盟类似):
1. 低风险:Class A/ Class A灭菌/Class A(测量)/Class A重复使用手术器械
2. 中低风险:Class B
3. 中高风险:Class C
4. 高风险:Class D
IVD分类:
1. 个人风险低,公共卫生水平低风险:Class A
1. 个人风险中等,公共卫生水平低风险:Class B
2. 个人风险高,公共卫生水平中等风险:Class C
3. 个人风险高,公共卫生水平高风险:Class D
根据沙特阿拉伯医疗器械法规,SFDA接受将主型号、相关型号、附件作为组合到一个单独申请中。在沙特阿拉伯销售之前,设备必须在参考国家(澳大利亚、加拿大、欧洲、日本或美国)获得授权。对于参考国家的边界产品和不同类别的器械,SFDA有正式分类的规定(可咨询欧必美)。
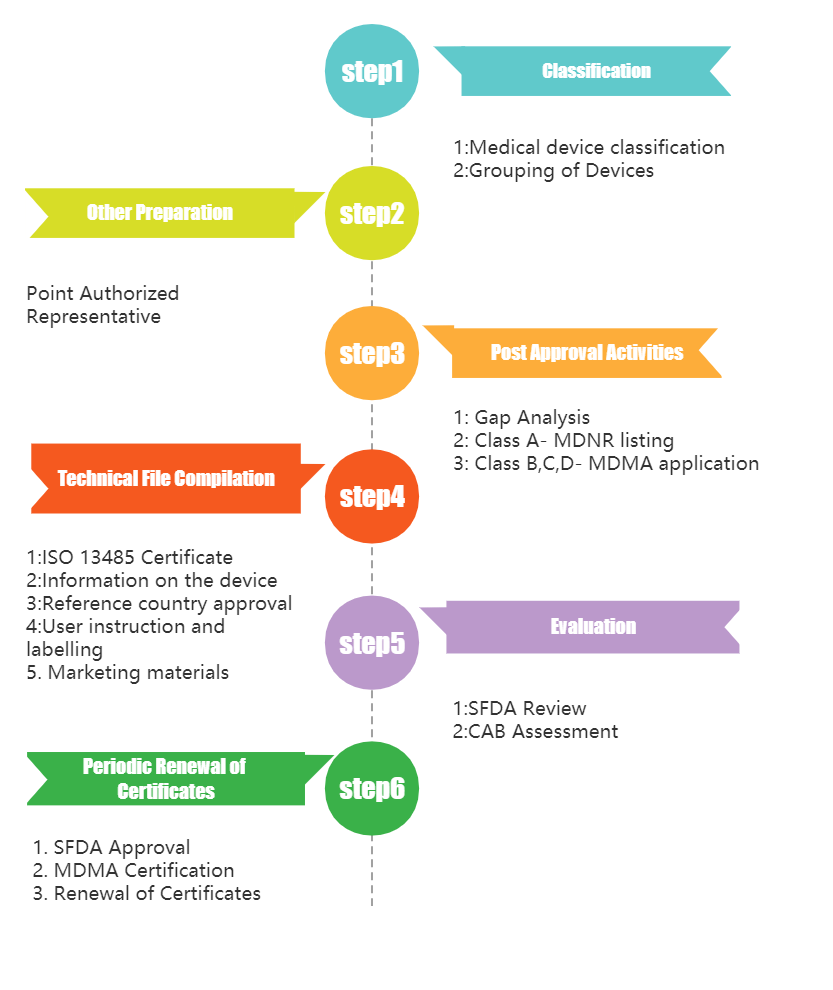
三、认证模式
沙特阿拉伯医疗器械注册要求因器械类别而异,有两种医疗器械审批途径,例如:
1. 医疗器械国家注册处 (MDNR) 列示
I 类普通的医疗器械需要在医疗器械国家注册处 (MDNR) 中列出,作为在 KSA 销售该设备的先决条件。此路径需要基本产品和制造商信息、QMS 证明、参考国家批准、IFU、标签和销售材料以及其他要求。SFDA通过该途径批准医疗器械的时间为4个工作日,有效期为3年。
2. 医疗器械上市许可 (MDMA)
所有其他类别的设备必须获得作为医疗设备上市许可 (MDMA) 颁发的医疗设备认证,才能在 KSA 销售设备。通过该途径获得 MDMA 批准的 SFDA 医疗器械注册时间通常为 35 天,许可证有效期为原始许可证有效期或未定义的原始许可证有效期为 3 年。